| La bioactivación |
 |
Diversas partes de este proceso tóxico común, revisten
una especial importancia.
La bioactivación es uno de ellos. Numerosos productos químicos
no actúan directamente, sino que son sus metabolitos, formados
endógenamente en el hígado y otros tejidos, los últimos
responsables de la toxicidad.
Por ello el procesado metabólico de los productos químicos
reviste la máxima importancia por cuanto es uno de los factores
que determina la dosis efectiva y la magnitud del efecto.
 |
Figura 2:
Fase I y II de la biotransformación
de los productos químicos. En cada etapa intervienen
distintos grupos enzimáticos codificados por genes específicos.
AGT: Transferasas del ácido glucurónico; GST:
transferasas del glutation; NAT: N-acetil transferasas. |
Se lleva a cabo habitualmente en etapas consecutivas (fig 2), donde
intervienen numerosos enzimas de fase I, como el sistema citocromo
P450 o epóxido hidrolasas (figs 3 y 4), La fase I puede generar
metabolitos reactivos (electrófilos, radicales libres), con
apetencia por dianas celulares.
 |
Figura 3:
Tipos de reacciones oxidativas
catalizadas por el sistema citocromo p450 en el hígado
u otros tejidos. |
 |
Figura 4:
Ciclo de funcionamiento
de sistema p450 microsomal (oxidasa de función mixta)
que resulta en la oxidación de numerosos substratos exógenos. |
La fase 2, habitualmente detoxificadora, conjuga los metabolitos
resultantes de la fase I con productos del metabolismo intermediario
como el glutation (fig 5) o el ácido glucurónico (fig
6).
 |
Figura 5:
Glutation: tripéptido
utilizado como cofactor en numerosas reacciones detoxificadoras.
Presenta además distintas funciones biológicas
como protector de membrana y regulador de cisteína. |
 |
Figura 6:
Conjugación con
ácido glucurónico: una de las habituales reacciones
dotoxificadoras de Fase II |
Cada una de estas categorías está constituida por
familias de isoenzimas, con afinidades distintas por diversos substratos,
y finamente regulada su concentración y actividad a nivel
genético.
Habitualmente la fase 2 es desactivadora y genera conjugados, como
los derivados de la N-acetilcisteína, inertes y fácilmente
eliminables dada su elevada hidrosolubilidad (fig 7).
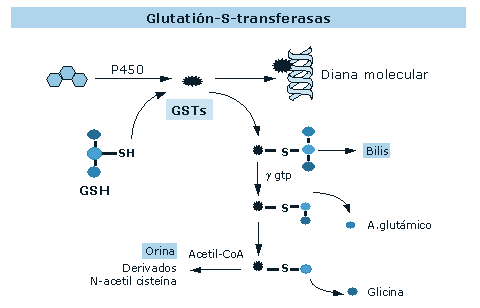
 |
Figura 7:
Conjugación
con glutation y eliminación del producto tóxico
en forma de derivados inertes de la N-acetilcisteína.
El balance entre bioactivación de Fase I y desactivación
de Fase II crítico en la génesis de la toxicidad. |
El balance entre la formación de metabolitos reactivos en
la fase I y su desactivación en la fase II, es crítica
en la génesis de numerosos efectos tóxicos y carcinogénicos.
Así, un malfuncionamiento de esta fase II o el agotamiento
de cofactores para la conjugación, es un aspecto decisivo
en la hepatotoxicidad de productos como el paracetamol, en los que
la toxicidad se encuentra mediada por la interacción de metabolitos
reactivos resultantes de una bioactivación de fase I con
determinadas proteínas hepáticas(fig 8).
 |
Figura 8:
Metabolismo y bioactivación
del paracetamol hasta formar un metabolito electrófilo
(N-acetilbenzoquinoneimina). |
|